Con receta Médica. Uso hospitalario. Reembolsado por el SNS. PVLn REVOLADE 25 MG 28 COMPRIMIDOS 843,62 €. PVLn REVOLADE 50 MG 28 COMPRIMIDOS 1.687,24 €. PVLn REVOLADE 25 MG 30 SOBRES SUSPENSION ORAL 903,4 €.
Con receta Médica. Uso hospitalario. Reembolsado por el SNS. PVLn REVOLADE 25 MG 28 COMPRIMIDOS 843,62 €. PVLn REVOLADE 50 MG 28 COMPRIMIDOS 1.687,24 €. PVLn REVOLADE 25 MG 30 SOBRES SUSPENSION ORAL 903,4 €.
En pacientes con aplasia medular grave (AMG) adquirida refractaria
REVOLADE® proporciona una respuesta multilínea1
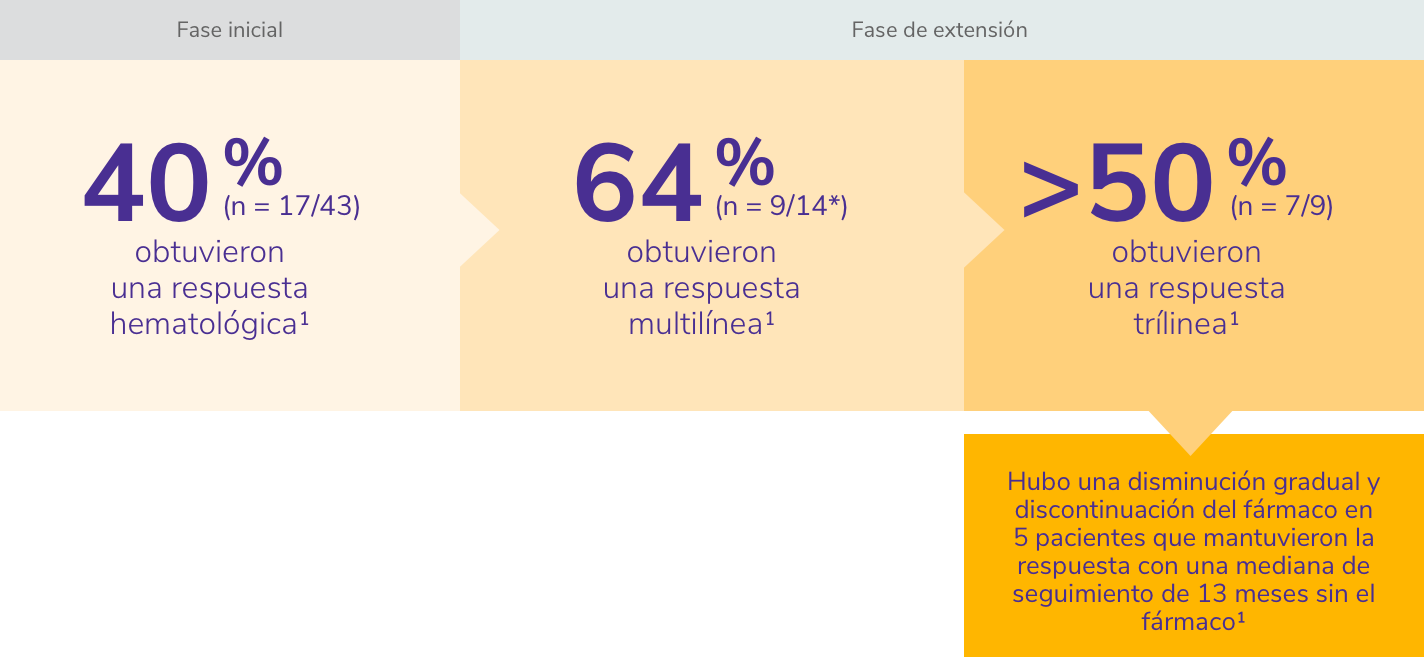
*Tres de los 17 pacientes aptos no iniciaron la fase de extensión1.
La variable principal fue la respuesta hematológica valorada después de 12-16 semanas de tratamiento con REVOLADE®.
La respuesta hematológica se definió como el cumplimiento de uno o más de los siguientes criterios:
|
|
Incremento de ≥20.000/μL plaquetas respecto a valores inicialesoIndependencia transfusional ≥8 semanas en pacientes inicialmente dependientes. |
|
|
Incremento del nivel de hemoglobina (si el nivel inicial <9 g/dL) de ≥1,5 g/dL sin transfusionesoReducción del número de concentrados de hematíes transfundidos de ≥4 concentrados en 8 semanas consecutivas, comparado con los requerimientos de las 8 semanas anteriores al inicio del estudio. |
|
|
Incremento del ≥100 % en el RAN en pacientes con un valor inicial basal de <500/μL.oUn incremento de RAN de >500/μL en pacientes con un RAN de ≥500/μL inicial. |
Los pacientes que respondieron podrían continuar la terapia en una fase de extensión.
El tratamiento con REVOLADE® se asoció a independencia transfusional de plaquetas y hematíes2
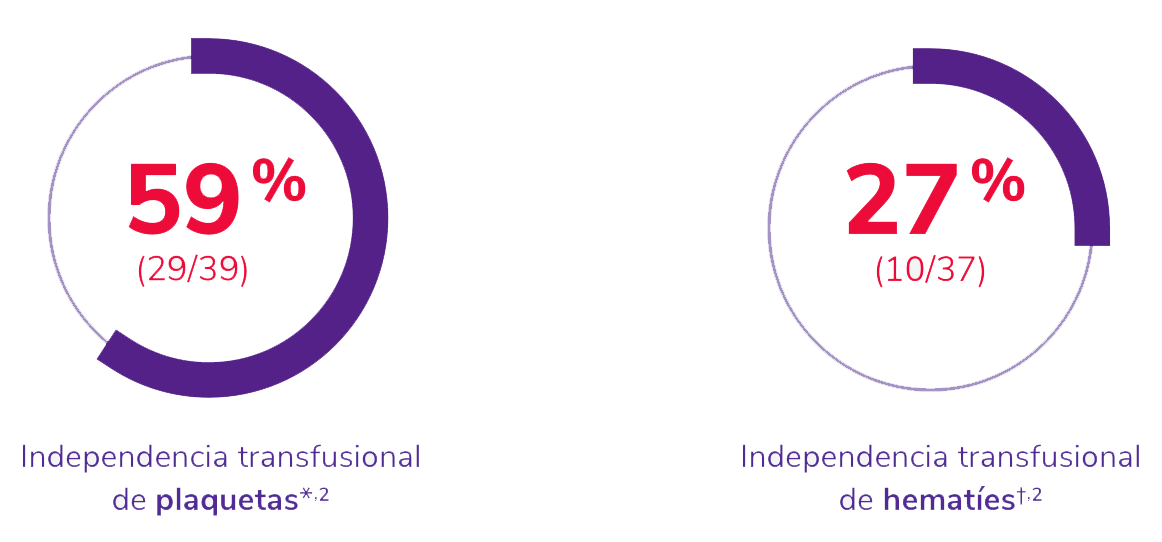
*El 91 % de los pacientes eran dependientes de transfusiones de plaquetas al inicio del estudio (39/43).
†El 86 % de los pacientes eran dependientes de transfusiones de hematíes al inicio del estudio (37/43).
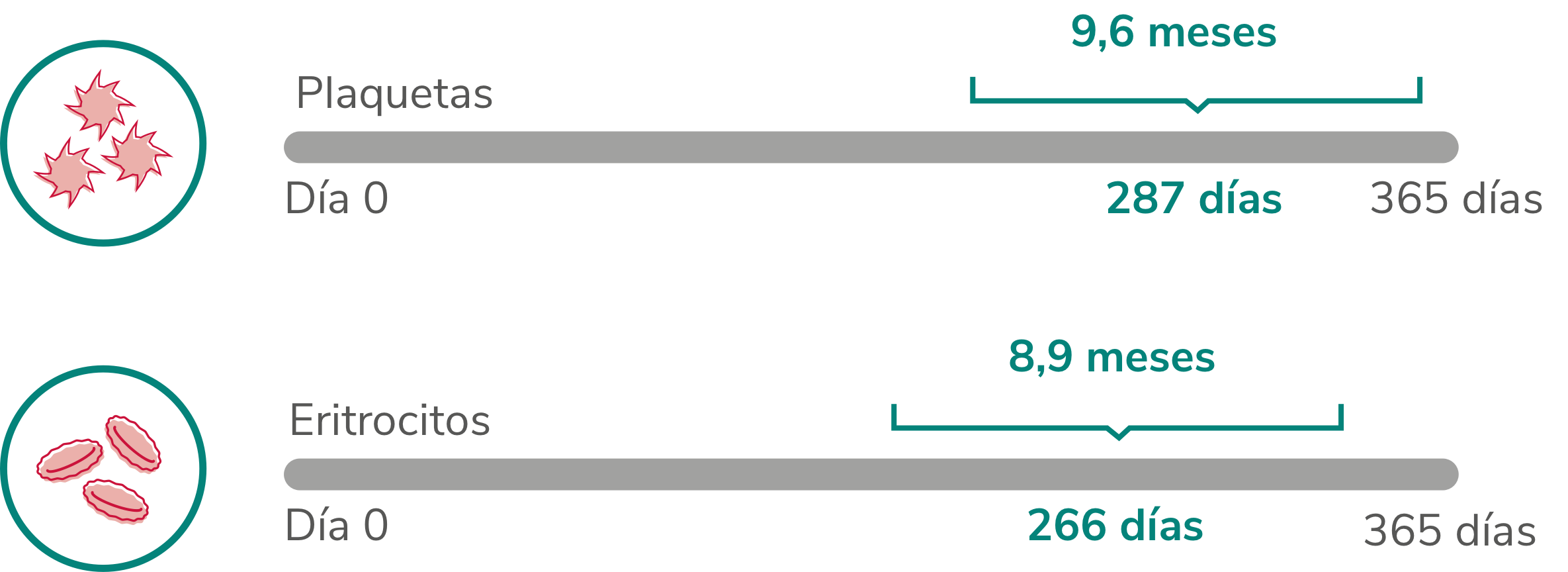
La respuesta con REVOLADE® en monoterapia permitió a los pacientes permanecer libres de transfusiones durante aproximadamente 9 meses2
Mediana del periodo sin transfusiones en respondedores2
Estudios de REVOLADE® en aplasia medular grave (AMG)
Estudio en AMG refractaria2-4
Estudio fase 2, pivotal no aleatorizado iniciado por investigador (n = 43) para evaluar la seguridad y respuesta hematológica en pacientes con AMG refractaria y describir la duración y calidad de las respuestas, el impacto de la discontinuación en respondedores robustos y la incidencia de evolución clonal.
- Incluyó a 43 pacientes ≥12 años de edad con AMG refractaria después de al menos un tratamiento inmunosupresor previo y con un recuento de plaquetas ≤ 30.000/μL.
- La variable principal fue la respuesta hematológica valorada después de 12-16 semanas de tratamiento con REVOLADE®. La respuesta hematológica se definió como el cumplimiento de uno o más de los siguientes criterios:
|
|
Incremento de ≥20.000/μL plaquetas respecto a valores inicialesoIndependencia transfusional ≥8 semanas en pacientes inicialmente dependientes. |
|
|
Incremento del nivel de hemoglobina (si el nivel inicial <9 g/dL) de ≥1,5 g/dL sin transfusionesoReducción del número de concentrados de hematíes transfundidos de ≥4 concentrados en 8 semanas consecutivas, comparado con los requerimientos de las 8 semanas anteriores al inicio del estudio. |
|
|
Incremento del ≥100 % en el RAN en pacientes con un valor inicial basal de <500/μL.oUn incremento de RAN de >500/μL en pacientes con un RAN de ≥500/μL inicial. |
Los pacientes que respondieron podrían continuar la terapia en una fase de extensión
Referencias:
1. Desmond R, et al. Eltrombopag restores trilineage hematopoiesis in refractory severe aplastic anemia that can be sustained on discontinuation of drug. Blood. 2014;123(12):1818-1825.
2. Ficha técnica de REVOLADE®.
3. Olnes MJ, et al. Prevalence and treatment of chronic idiopathic thrombocytopenic purpura of childhood in Sweden. Acta Paediatr. 1997;86(2):226-7.
4. Desmond R, et al. Eltrombopag restores trilineage hematopoiesis in refractory severe aplastic anemia that can be sustained on discontinuation of drug. Blood. 2014;123(12):1818-1825.